准教授・井上克枝 (Katsue Suzuki-Inoue)
 内科医。英国Oxford大学留学中よりコラーゲン受容体による血小板活性化機序に関する研究を行ってきたが、血小板が活性化する(又は活性化抑制でも可)メカニズムなら何でも興味の対象になってしまうため同時進行中の研究を多数抱えこんでいる。さらに大学院生時代に魅了された血小板を活性化する蛇毒・ロドサイチンの受容体として2006年に新規血小板活性化型受容体CLEC-2を同定し、2007年には、CLEC-2の生理的なリガンドとして腫瘍抗原のポドプラニンを同定した事から、研究範囲が腫瘍と血小板の関係にまで拡大し、超過勤務の日々を送ってきた。
内科医。英国Oxford大学留学中よりコラーゲン受容体による血小板活性化機序に関する研究を行ってきたが、血小板が活性化する(又は活性化抑制でも可)メカニズムなら何でも興味の対象になってしまうため同時進行中の研究を多数抱えこんでいる。さらに大学院生時代に魅了された血小板を活性化する蛇毒・ロドサイチンの受容体として2006年に新規血小板活性化型受容体CLEC-2を同定し、2007年には、CLEC-2の生理的なリガンドとして腫瘍抗原のポドプラニンを同定した事から、研究範囲が腫瘍と血小板の関係にまで拡大し、超過勤務の日々を送ってきた。
ポドプラニンはリンパ管内皮マーカーとしても有名であるが、なぜリンパ管内皮に血小板のリガンドが?と疑問に感じ、かねてより「血管とリンパ管の分離部位ではCLEC-2を介して血小板が活性化され、血栓が出来ていたりしてね」と冗談めかしていたが、実は本当らしい事がCLEC-2欠損マウスの検索等から判明した。結果、現在はリンパ管分野にも研究領域が拡大。多正面作戦でCLEC-2の研究に挑んでいる。
プライベートでは2児の母。第2子誕生後、好きなサイクリングの再開見通しがますます遠のき、愛車は静態保存中。牛歩の歩みでしか進まない研究の重圧とダッコを奪い合う2児の圧倒的なパワーに翻弄され、補中益気湯で疲れた体に活を入れる日々が続く。
所属 : 大学院総合研究部 医学学域 臨床医学系(臨床検査医学)
医学部 臨床検査医学講座
学歴 : 1995年3月 山梨医科大学医学部 卒業
2001年3月 山梨医科大学大学院 修了
学位 : 博士(医学) ( 山梨大学 )
資格 : 日本臨床検査医学会認定 臨床検査管理医
- 同 臨床検査専門医
職歴 : 1995年5月 東京厚生年金病院 内科 研修医
2000年4月 山梨医科大学助手(臨床検査医学)
2001年4月 University of Oxford, U.K., Post doctoral researcher. (〜2003年3月末)
2002年10月 山梨大学助手(臨床検査医学講座)
2006年1月 山梨大学講師(臨床検査医学講座)
2007年7月 山梨大学医学部准教授(臨床検査医学講座)
2016年1月 山梨大学大学院総合研究部医学域臨床医学系教授(臨床検査医学講座)
所属学会 : 日本内科学会
日本血栓止血学会・評議員/編集委員
日本血液学会
日本臨床検査医学会
日本臨床検査専門医会
International Society on Thrombosis and Haemostasis
American Society of Hematology
American Society for Biochemistry and Molecular Biology
受賞 : <<研究活動に対する受賞>>
- 若手研究者表彰 ( 山梨医科大学医学会 ) ( 2001年 )Young Investigator Travel Award ( XVIII Congress, ISTH ) ( 2001年 )
- Merit Award ( University of Oxford, Department of Pharmacology ) ( 2001年 )
- 平成16年度血栓止血学会学術奨励賞 ( 日本血栓止血学会 ) ( 2004年 )
- 山梨科学アカデミー奨励賞 ( 山梨科学アカデミー ) ( 2005年 )
- Young Investigator Award 優秀賞 ( 第5回血液血管オルビス ) ( 2007年 )
- Papers of the Week ( Journal of BIological Chemistry ) ( 2007年 ) ( 山梨日日新聞,NHK山梨放送局より報道 ) 等
- Young Investigator Award ポスターセッション最優秀賞 ( 第7回血液血管オルビス ) ( 2009年 )
- Papers of the Week ( Journal of BIological Chemistry ) ( 2010年 )
- Young Investigator Award 最優秀賞 ( 第8回血液血管オルビス ) ( 2010年 )
血小板活性化受容体 CLEC-2
研究者生命(と獲得した研究資金)をかけた魂のプロジェクト
CLEC-2は "C-type lectin-like receptor 2" の略です。CLEC-2は血小板ー巨核球系と、腎臓の足細胞、肝臓の類洞上皮細胞に発現が見られますが、その生理的な役割はあまり解明されていません。私はこのCLEC-2の生理的役割の解明をテーマに研究活動を展開しています。
私たちは、2003年に留学先の英国人ボスであるSteve. P. Watson博士(現英国Birmingham大教授)とポスドク仲間のAngel Garcia博士 (現スペインSantiago de Compostela大学・エンジェルではなくアンカハルと発音します)らの協力の下、血小板活性化蛇毒 "rhodocytin" を用いて血小板膜上に発現するCLEC-2の同定に成功しました。その後CLEC-2下流のシグナル伝達機構を解析し、2006年に新規血小板活性化受容体として初めて血小板CLEC-2を世界に報告しました。当初は生体内リガンドが不明のorphan receptorであったCLEC-2ですが、2007年には国内研究者らとの共同研究により生体内リガンドの特定に成功、2009年にはCLEC-2欠損マウスの作製にも成功するなど、CLEC-2の研究に於いては独自のポジションを築いてきました。現在はアメリカ、イギリス、ドイツの研究チームとcompetitiveな状況にありますが、日本から世界に向け、CLEC-2に関する情報を発信し続けるべく奮闘中です。
血小板膜上にはいろいろな血小板活性化受容体が発現しています。これは生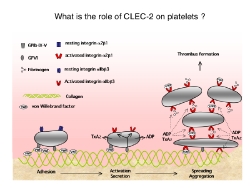 動脈硬化/血栓性疾患ハンドブックより引用改変命の進化の歴史が弱肉強食の連続だったことに由来すると想像されます。血管壁が傷害され出血した際も、速やかに止血されなくては生き延びる事が出来ない。この生存競争を勝ち抜いてきたヒトには、止血を担う血小板に多種の活性化受容体が多数発現しています。CLEC-2もそんな血小板活性化受容体の一つです。実際に血小板活性化シグナルを出し凝集塊を形成止血血栓を形成できるCLEC-2は、それまで知られていたADP受容体やThrombin受容体、Thromboxan A2受容体などの7回膜貫通型受容体やコラーゲン受容体Glycoprotein VI (GPVI)やFcgammaRIIAなどのimmunoglobulin super familyとは異なるC-type lectin super familyに属し、生理的役割は全く解明されていない未知の受容体でした。しかしCLEC-2は巨核球-血小板系に比較的特異性を持った発現をしており、抗血小板薬の標的蛋白として有望ではないかと予想されます。
動脈硬化/血栓性疾患ハンドブックより引用改変命の進化の歴史が弱肉強食の連続だったことに由来すると想像されます。血管壁が傷害され出血した際も、速やかに止血されなくては生き延びる事が出来ない。この生存競争を勝ち抜いてきたヒトには、止血を担う血小板に多種の活性化受容体が多数発現しています。CLEC-2もそんな血小板活性化受容体の一つです。実際に血小板活性化シグナルを出し凝集塊を形成止血血栓を形成できるCLEC-2は、それまで知られていたADP受容体やThrombin受容体、Thromboxan A2受容体などの7回膜貫通型受容体やコラーゲン受容体Glycoprotein VI (GPVI)やFcgammaRIIAなどのimmunoglobulin super familyとは異なるC-type lectin super familyに属し、生理的役割は全く解明されていない未知の受容体でした。しかしCLEC-2は巨核球-血小板系に比較的特異性を持った発現をしており、抗血小板薬の標的蛋白として有望ではないかと予想されます。
血小板の仕事は当然血栓止血、と言う観点から血小板CLEC-2は”血栓症治療のための抗血小板薬の標的蛋白として有望であろう”と研究を行ってはきましたが、最近の研究からは、
1.血小板CLEC-2は一部の腫瘍において、その遠隔転移を促進する分子であること
2.血小板CLEC-2は胎生期のlymphangiogenesisに関わること
など、今までの血小板の役割の概念を超えた、血小板の新たな役割も浮かび上がってきています。血小板は出血部位での血栓止血や病的血栓形成以外にも生体内で重要な役割を担っているのです。現在の研究は血小板CLEC-2を標的とした、新たな抗腫瘍薬や抗転移薬の開発につながるのではないかと期待しています。
CLEC-2に関する研究成果はこれまで2回 JBC誌のPapers of the Weekに選ばれております。これは彼の地でCLEC-2がいかに興味を持って捉えられているかを示しています。現に私たちと同じような研究を行っているグループが欧米にはわかっているだけで既に3グループあります。2グループは後発組ですが、すでにCLEC-2を欠損させる実験系を確立しています。英国でのポスドク生活で垣間見た、英語圏の研究者間の情報ネットワークや大学の資金力は、それはそれはすごいものです。論文のデータ等の意見交換も国際電話でホイですし、日本と異なり研究室にはミニラボヘッドにようなポスドクやフルタイムの大学院生が沢山います。アメリカ人ポスドクが帰国と同時に最新式の実験装置を導入して研究を始めるのを羨ましく思ったりもしました。環境の異なる日本で研究を行い、世界に向けて情報を発信してゆくには、共同研究の形でお互いの不得意分野を補ってゆく道しかありません。というわけで、CLEC-2の研究ではいつもいろいろな大学の先生方にお世話になっております。無理を聴いて下さる共同研究者の諸先生方には感謝の毎日です。ありがとうございます。
さて、本題に戻りますが、CLEC-2は血栓症や悪性腫瘍の遠隔転移の予防的治療の標的分子として有望であろうということで、企業や研究者の興味の対象となっているのが現状です。
私のコーナーでは、血小板CLEC-2に関する私たちの研究の一端をご紹介し、新たな研究成果についても適時情報発信してゆきたいと思います。
血小板CLEC-2とそのリガンド
蛇毒蛋白の中には、血小板を活性化し、凝集反応を惹起させる物があります。
マレーまむしの蛇毒蛋白rhodocytin(rhod)もその一つです。血小板をバッファに浮遊させた血小板浮遊液にrhodを添加すると、多少のタイムラグを経て強い凝集反応が観察されます。ということは血小板膜上にrhodを認識する受容体があると言うことになりますが、私が実験を始めた20世紀末にはこのrhodocytin受容体は同定されていませんでした。未知の受容体か?幸い私たちのラボは明治薬科大学の森田先生研究室から精製したrhodを分与していただくことができ、rhodを使った実験が可能な状況でした。当時大学院生だった私は、細々したプロジェクトを走らせては居ましたが、“rhodocytinを認識する血小板膜上受容体を探し”はとても魅力的なプロジェクトに思え、尾崎教授に相談の上、自分のテーマとして研究を開始する事にしました。
戦略としては、先ずは既知の血小板膜受容体がrhococytin受容体である可能性を検討します。既知の血小板活性化受容体の中でrhodの受容体候補として考えたのはコラーゲン受容体のintegrin alpha2beta1でした。同じコラーゲン受容体glycoprotein VI/Fc receptor gamma (GPVI/FcRgamma)欠損マウス血小板はrhod刺激で凝集しますが、integrin alpha2beta1を阻害抗体でブロックするとrhod惹起血小板凝集が強く抑制される事、またrhodを結合させたリポソームがintegrin alpha2beta1に結合することから、自信を持ってJBC誌に発表しました(Suzuki-Inoue et.al., J.Bio.Chem. 276:1643-1652, 2001)。
ところが、、
同じ時期に同じことをしている研究者が世界中には複数いることを初めて思い知りました。なんとrhodcytinの受容体に関する相反する論文があいつで発表されたのでした()。integrin alpha2beta1とGPIbのダブル欠損マウスでも血小板凝集が惹起されるとの報告に、これまでの研究成果を否定されたような気分になり、しばらくrhodocytin関連の研究からは足が遠のいてしまいました。
Rhodocytinのリガンド探しに再度挑む気になったのは、イギリス留学中のことです。当時Oxford大学のSteve P. Watson博士の研究室でポスドクをしていた私に、Steveがリガンド探しの研究再開を勧めました。Steveのラボとその周りのラボには、ヨーロッパを中心にいろいろな特技を持つポスドクが集っていました。彼らの中にはproteomicsの専門家も居り、共同研究でrhodocytin受容体探しを再開する事となりました。院生時代の自分の研究を全否定された様な気分でしばらくrhodネタから逃避していた私ですが、研究に専念できるイギリスでのポスドク生活ですっかり元気になり、取組前から気合いは十分です。
ちょうど研究プロジェクトが始まった頃に、山梨大学の研究室の事情から予定より早く呼び戻されたため、このプロジェクトは山梨を中心とした多国間での共同研究という形を取ることになりました。
さて血小板膜上のrhococytin受容体をどう回収するか?
私のいる山梨大学臨床検査医学講座はsignal屋を自認しており、免疫沈降で目的の蛋白を釣ってくるのは得意です。私もその端くれですから、この方法を利用して膜蛋白を釣ってくることにしました。
概要ですが、まずはrhococytinをCNBrビースに固相化します。コントロール用にグリシンをくっつけたビースも作ります。これは簡単。次に血小板膜状の蛋白をbiotin化しておきます。これも簡単。そしてこれを溶解し血小板lysateを作りrhococytinビーズまたはグリシンビースと混ぜ合わせます。その後遠心してビーズを回収、くっついてきた膜蛋白を電気泳動で分離し、PVDF膜に転写します。 この後は通常のwestern blotを行います。膜蛋白にはbiotinがくっついているので、streptoavidin-HRPと反応させ発色させ、コントロールビースのサンプルにはなくrhodocytinビースのサンプルには認められるバンドがあれば、これがrhodocytinに結合する膜蛋白を含むバンド、ということになります。同じゲル上に同時にbiotin化していないサンプルをもう一組泳動しておけば、目的のバンドと同じ分子量の部位のゲルを切り抜いて質量分析を行う事が出来ます。質量分析は自前では難しいので、蛋白屋であるポスドク仲間のスペイン人A. Garcia博士(現バルセロナ大学)にお願いする計画になっています。書けば簡単ですが、実際行うとやはり試行錯誤が必要でしたが、何度か繰り返す中に、(幸運なことに)ハッキリとしたバンドを32-kD付近に検出することができました。同じ部位は、rhod-biotinでwestern blotした場合も確認する事ができました。
この後は通常のwestern blotを行います。膜蛋白にはbiotinがくっついているので、streptoavidin-HRPと反応させ発色させ、コントロールビースのサンプルにはなくrhodocytinビースのサンプルには認められるバンドがあれば、これがrhodocytinに結合する膜蛋白を含むバンド、ということになります。同じゲル上に同時にbiotin化していないサンプルをもう一組泳動しておけば、目的のバンドと同じ分子量の部位のゲルを切り抜いて質量分析を行う事が出来ます。質量分析は自前では難しいので、蛋白屋であるポスドク仲間のスペイン人A. Garcia博士(現バルセロナ大学)にお願いする計画になっています。書けば簡単ですが、実際行うとやはり試行錯誤が必要でしたが、何度か繰り返す中に、(幸運なことに)ハッキリとしたバンドを32-kD付近に検出することができました。同じ部位は、rhod-biotinでwestern blotした場合も確認する事ができました。
どうやらこれは本物のようです。これで一気にrhod受容体同定の野望が現実味を帯びてきました。
質量分析は蛋白屋の腕の見せ所です。計画通りくり貫いたゲルをAngel Galcia博士(エンジェルではなく、アンカルと読みます。カはカとハを同時に発音する感じの破裂音。同世代です。)に送ります。あとは彼がこのゲルをMS/MS解析にかけ、可能性のある蛋白を(早急に)リストアップしてくれるはずです。早く結果が知りたいし、でも自分では解析できないし、と研究室内でウロウロソワソワ落ち着かない日日が続きます。頼むよAngel!落ち着かなくて全く仕事にならんよ!そんな私の心境を察知したのか、発送後2週間ほどたった頃にAngelから「返事が遅くなってるけど、丁寧にやっているからだよ。忘れて放ってあるわけじゃないよ。」との連絡が入ります。さすがは情熱の国スペインの男、研究においても女心のケアを欠かしません。さらに過ごすこと1週間、ゲルを発送して3週間後、Angelからのレポートが届きました。
ヒットした蛋白一覧から、さっそく膜蛋白を探します。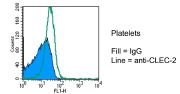 イ 血小板膜上にCLEC-2が発現C-type lectin-like receptor 2?なんだこれ??調べてみると、どうやら細胞内ドメインに、Y-x-x-Lという血小板コラーゲン受容体GPVI/FcRgでおなじみのモチーフが1つあるようです。Y-x-x-Lが2つあればITAM motifだから、1つしかないけど、うん、これに違いない。
イ 血小板膜上にCLEC-2が発現C-type lectin-like receptor 2?なんだこれ??調べてみると、どうやら細胞内ドメインに、Y-x-x-Lという血小板コラーゲン受容体GPVI/FcRgでおなじみのモチーフが1つあるようです。Y-x-x-Lが2つあればITAM motifだから、1つしかないけど、うん、これに違いない。
安直な発想ですが、C-type lectin-like receptor 2(CLEC-2)をrhod受容体候補の筆頭と決定しました。あとは検証作業です。
ア・CLEC-2発現細胞を用いてrhod-CLEC-2結合をflowcytometoryで確認。
イ・血小板膜上のCLEC-2蛋白発現をflowcytometryで再確認。
ウ・CLEC-2発現細胞をrhod刺激し、蛋白質チロシンリン酸化が増加するか検討。
エ・Rhod刺激により血小板CLEC-2自体がチロシンリン酸化されるか検討。
オ・抗CLEC-2抗体を用いてCLEC-2をクロスリンクすると血小板凝集か惹起されるか検討。
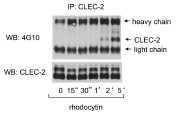 エ Rhod刺激による血小板CLEC-2のタンパク質チロシンリン酸化増加の様子
エ Rhod刺激による血小板CLEC-2のタンパク質チロシンリン酸化増加の様子
幸いにもこれらの検討にパスし、晴れてrhodocytinの血小板膜上受容体はC-type lectin-like receptor 2であることが確認されました。当初は懐疑的な目で見られていた日本人ボスからも、これ以後当プロジェクトには多少なりとも興味を持っていただけるようになりました。しかし、生体内のリガンドが不明のままでは、生体内に多数知られるophan receptorの1つという認識の域をでず、引き続き生体内リガンドを同定するプロジェクトに進むことにしました。
ここまでの研究成果は、下記論文へ掲載されました。
Suzuki-Inoue K et.al., A novel Syk-dependent mechanism of platelet activation by the C-type lectin receptor CLEC-2. Blood. 2006;107: 542-549.
CLEC-2欠損マウスの作製
CLEC-2の生体内リガンドを一つ発見し、報告出来た事は非常な幸運でしたが、podoplaninはリンパ管内皮や腎足細胞、腫瘍表面など血小板のリガンドとして生理的に血液に接する部位には発現していません。そのためCLEC-2の生理的役割の解明にはやはりCLEC-2欠損マウスを作製するしかありません。Rhodocytinと関わりを持った10年前からずっと消化不良のまま残っていた課題にいよいよ結論が出せる?
CLEC-2は自分の研究者生命をかけるにふさわしい、いわば「井上克枝・魂のプロジェクト」です。是非ともCLEC-2欠損マウスを作製し、生理的役割を知りたい。この計画は以前から温めており、2003年秋には自作のノックアウトベクターを作り始めたのですが、その後は作製に取り掛かるチャンスに恵まれませんでした。しかし今回は、期せずして選ばれたJBC・Papers of the Weekに自信を深め、教授にいろいろな可能性を説明し、度重なる交渉の末に本プロジェクトを実行に移すGOサインを得る事が出来ました。
しかし遺伝子改変マウスの作製は当研究室始まって以来初めての事です。また、資金面でも作製失敗は許されない額の経費が見込まれます。自分の獲得してきた研究資金を集計し、これを懐具合の目安にとにかく見積もりを取り、当初A社と契約しました。自前のノックアウトベクターを使ってES細胞に組み込むまでは良かったのですが、途中で評価系に不具合が判明し、頓挫。泣く泣くB社に乗り換え、始めからやり直す事になりました。その後も細かなトラブルが続きましたが、B社の協力もあり解決にこぎつけました。CLEC-2欠損マウスの作製に3年が費やされ、2009年春に待望のヘテロマウスが完成しました。苦節6年目の春でした。
なんとCLEC-2 nullマウスはほとんど生まれてこない
CLEC-2欠損マウスは胎生あるいは出生後極めて早期に死亡することが分かりました。ヘテロ同士の交配による胎仔の遺伝子型を見てみると、胎生13.5日まではほぼメンデルの法則通りですが、E15.5から徐々に減ってゆき、出生時には約10%となります。しかし、このほとんどのマウスは出生後極めて早期に死亡し、成獣になったのは326匹中2匹にすぎませんでした。
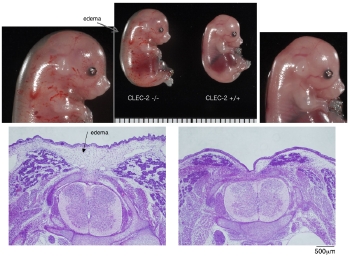
胎仔を観察すると、 CLEC-2 nullマウスでは全体に皮下出血様の発赤が目立ちます。しかしよく見ると、これは出血ではなく皮膚血管の拡張蛇行である事が分かりました。さらに胎仔は全体に浮腫が目立ち、HE染色標本でも皮下組織の浮腫状変化が確認できました。胎仔に何か起こっているのでしょうか?
数年前のScienceに、Dr. M.Kahnらの研究成果が発表されました。血球細胞に発現し、内皮細胞には発現していない細胞内シグナル分子SykとSLP-76の欠損マウス胎仔では胎仔皮膚と腸管に拡張した脈管が見られ、これらはリンパ管と血管の分離不全により生じたリンパ管の異常所見でリンパ管内にも血液が流れる状態である事を報告しました。つまりSykとSLP-76は血管とリンパ管の分離に必要なシグナル分子なのです。
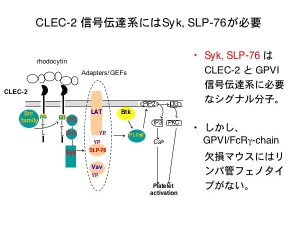
SykとSLP-76は血小板には豊富に存在し、CLEC-2やコラーゲン受容体GPVIによる血小板活性化機構に必須のシグナル分子です。しかしGPVI/FcR gamma chain欠損マウスでは、このような血管とリンパ管の異常症は認められません。と言う事は、CLEC-2が・・・?
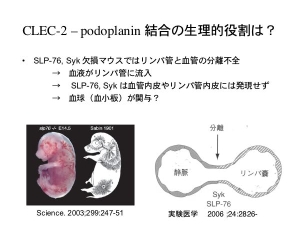
リンパ管内皮細胞により、CLEC-2 を介した血小板凝集が惹起されますが、生理的な状況ではリンパ管内皮のポドプラニンと血小板CLEC-2は接触する環境に併存しません。しかし、リンパ管は胎生期に血管より発生・分離し、独立した循環系を形成してゆきます。なのでリンパ管発生の段階では、血液とリンパ管は接触する可能性があるのではないか?
実際、ポドプラニン欠損マウスにはリンパ管発生異常があります。
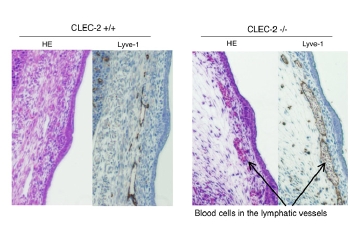
そこでCLE-2胎仔の薄切標本を作製し、HE染色とリンパ管を染めるLyve-1抗体で染色して観察してみます。すると、CLEC-2 nullの皮下には内部に赤血球を充満したLyve-1陽性の脈管(=リンパ管)が目立つ事がわかりました。
このようなリンパ管であるため、CLEC-2 nullでは組織液のドレナージ機能は大変損なわれています。胎仔前肢手背に注入した色素も、いつまで経ってもリンパ管に入ってゆきません。このためにCLEC-2 nullでは著明な浮腫が出現するのだろうと考えられます。
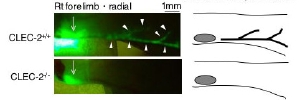
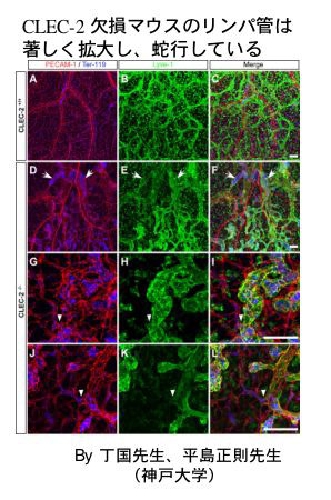
共同研究中の神戸大学平島正則先生、丁国先生らに胎仔皮膚の脈管をwhole mount法で染色して頂きましたことろ、やはり予想通りの結果が得られました。
赤がPECAM-1, 青が赤血球マーカーのTer-119、緑がLyve-1です。
マージしたものをみると、ノックアウトマウスでは青と緑が共存しており、リンパ管内に赤血球が混入していることが分かります。また、ノックアウトマウスのリンパ管は著しく拡張・蛇行しています。高倍率の写真をよく見ると、ノックアウトマウスの脈管には血管とリンパ管の繋ぎ目が何箇所か認められます。
これらの結果から、CLEC-2欠損によりリンパ管と血管の分離不全が生じ、血液がリンパ管に流入するという異常所見を呈する事、血管とリンパ管が交通するためにリンパ管内圧が高くなり、リンパ管の拡張・蛇行・ドレナージ機能不全が発生する事が示唆されます。
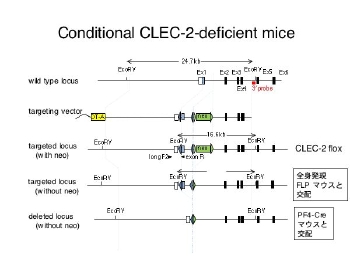 CLEC-2 は、マウスでは好中球にも発現しています。血小板上のCLEC-2 ではなく、好中球のCLEC-2 がリンパ管・血管分離を制御している可能性はどうでしょうか?この検討のために、血小板・巨核球系でのみCLEC-2 を欠損するマウスを作製しました。
CLEC-2 は、マウスでは好中球にも発現しています。血小板上のCLEC-2 ではなく、好中球のCLEC-2 がリンパ管・血管分離を制御している可能性はどうでしょうか?この検討のために、血小板・巨核球系でのみCLEC-2 を欠損するマウスを作製しました。
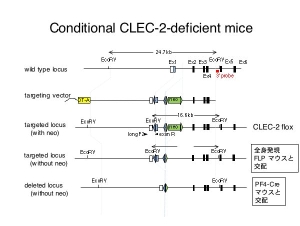
Null マウスを作製した時と同じ targeted allele をもつマウスを全身発現 FLTマウスと交配し、FRT で挟まれた neo 部分を除去します。さらに、PF4-Cre トランスジェニックマウスと交配して血小板・巨核球でのみCLEC-2を欠損したマウスを作製しました。
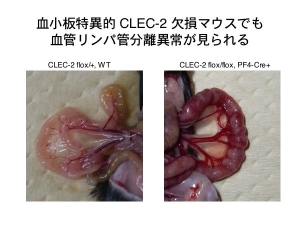 こうして作製したPF4-Creマウスは、CLEC-2 nullマウスと比較して胎仔生存率が多少高いのですが、やはり理論通りではありません。生き延びたマウスを解剖してみると、腸管にはCLEC-2 nullマウスの場合やSyk、SLP-76欠損マウスの場合と同様に、網目状の赤い拡張脈管が認められます。内部に血液を含むリンパ管である事も確認がとれました。
こうして作製したPF4-Creマウスは、CLEC-2 nullマウスと比較して胎仔生存率が多少高いのですが、やはり理論通りではありません。生き延びたマウスを解剖してみると、腸管にはCLEC-2 nullマウスの場合やSyk、SLP-76欠損マウスの場合と同様に、網目状の赤い拡張脈管が認められます。内部に血液を含むリンパ管である事も確認がとれました。
以上の所見から、血小板膜上のCLEC-2はリンパ管の発生、特に胎生期に血管から分離する際に重大な役割を演じている事が示唆されます。恐らく分化しポドプラニンを発現したリンパ管内皮細胞周囲で血小板が活性化され、血栓となり、血管とリンパ管の交通部位を閉塞するのでしょう。
この仮説は、2010年1月Bloodに"Novel function for blood platelets and podoplanin in developmental separation of blood and lymphatic circulation" ( Pavel Uhrin et.al., online Jan 28, 2010) が発表され、ほぼ正しかった事が証明されました。さらに3月にはCirculation Researchに”Platelets Play an Essential Role in Separating the Blood and Lymphatic Vasculatures During Embryonic Angiogenesis" (Laura Carramolino et.al., online March 4, 2010) が報告されました。どちらも胎仔の総静脈管とそこから分離したリンパ嚢の交通部分に血栓が出来ている像を、神技を駆使して組織学的に示しています。すごいです。素晴らしい。先を越されて残念なのですが、少しすっきりしました。今まで本気で取り合ってくれなかった教授が急にまともに聞いてくれるようになるという副次的な効果もありました。
その後、この仮説はTuomas Tammela と Kari Alitaloによるレビュー "Lymphangiogenesis: Molecular Mechanisms and Future Promise "(Cell 140, February 19, 2010) にも取り上げられ、ほぼ市民権を得た感じです。
しかし、同じような事を考えるヒトはいるものだなと思います。次は一番乗りしたいものです。
後に続けとばかりに急いで自分達もデータをまとめ発表しましたので、良かったらご覧下さい。
Suzuki-Inoue et.al., JBC, 2010
CLEC-2欠損マウスの解析
血栓止血における役割も検討しました。
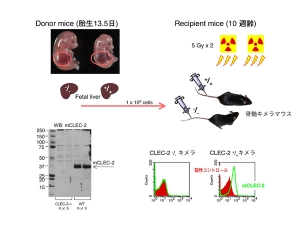 CLEC-2 nullマウスは出来たものの、ほとんど生まれてきません。また、運良く出生しても成体まで生存する確率は、1/200程度か、もっと低い数字です。これはCLEC-2が生存に重要な分子である事を示しているので、苦労して作って何もフェノタイプが無かった場合より喜ぶべき事なのですが、実際問題としてCLEC-2 nullの成体を使って血小板CLEC-2の役割を解析する事が出来ません。ただ、幸いなことに胎仔は胎生13.5日までは生存しています。
CLEC-2 nullマウスは出来たものの、ほとんど生まれてきません。また、運良く出生しても成体まで生存する確率は、1/200程度か、もっと低い数字です。これはCLEC-2が生存に重要な分子である事を示しているので、苦労して作って何もフェノタイプが無かった場合より喜ぶべき事なのですが、実際問題としてCLEC-2 nullの成体を使って血小板CLEC-2の役割を解析する事が出来ません。ただ、幸いなことに胎仔は胎生13.5日までは生存しています。
そこで胎仔の肝細胞を用いて骨髄キメラマウスを作製する事にしました。この方法は、放射線照射により骨髄を破壊した健常マウスに、胎仔の肝細胞を尾静脈より注射し、骨髄移植を行う方法です。胎生13.5の胎仔肝臓には造血細胞が多く含まれるため、CLEC-2 null胎仔の肝臓を取り出して細胞をバラバラに処理し、これを移植する事で、骨髄のみCLEC-2遺伝子が欠損したCLEC-2欠損骨髄キメラマウスが作製できます。実施にあたっては、東京大学医科学研究所・江藤浩之先生の研究室にお邪魔し手技操作等を御指導いただきました。ありがとうございました。
 各種アゴニスト刺激による血小板凝集反応 さて、このようにして作製したCLEC-2欠損骨髄キメラマウスでは、血小板上にCLEC-2の発現を認めません。また、当然ですが、CLEC-2刺激薬Rhodocytinでの刺激に血小板は反応せず、凝集が惹起されません。このマウスを用いて、血小板CLEC-2の血栓止血における役割に迫ってみました。
各種アゴニスト刺激による血小板凝集反応 さて、このようにして作製したCLEC-2欠損骨髄キメラマウスでは、血小板上にCLEC-2の発現を認めません。また、当然ですが、CLEC-2刺激薬Rhodocytinでの刺激に血小板は反応せず、凝集が惹起されません。このマウスを用いて、血小板CLEC-2の血栓止血における役割に迫ってみました。
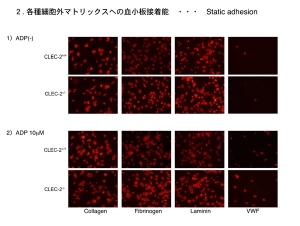 各種細胞外物質への血小板接着 血小板の主戦場は血栓止血の場面ですから、血管壁が傷害され内皮下組織が露出すると、そこに血小板が接着(adhesion)し活性化され、葉状仮足を出し変形し(spreadingし)、凝集塊を形成し、止血血栓や病的血栓を形成する、などと言った現象が惹起されます。この現象にCLEC-2の有無で差異が生じないか検討しました。
各種細胞外物質への血小板接着 血小板の主戦場は血栓止血の場面ですから、血管壁が傷害され内皮下組織が露出すると、そこに血小板が接着(adhesion)し活性化され、葉状仮足を出し変形し(spreadingし)、凝集塊を形成し、止血血栓や病的血栓を形成する、などと言った現象が惹起されます。この現象にCLEC-2の有無で差異が生じないか検討しました。
内皮下組織を言えばコラーゲンとラミニンですが、キメラマウス血小板は健常血小板とCLEC-2欠損血小板でadhesion、spreading共に明らかな差異が認められません。CLEC-2はコラーゲン受容体でもラミニン受容体でもないので、当然と言えば当然の結果です。
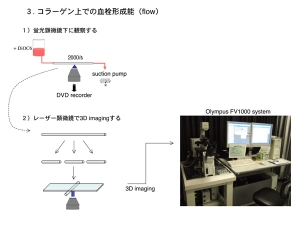 次に、生体内の環境を模して流速のある条件で血小板接着や血栓形成の様子を観察します。これは抗凝固剤と蛍光色素で処理したキメラマウス血液を、コラーゲンを固相化したガラスキャピラリーチューブ内に流し、血栓が形成される様子を見る実験系です。血液を流す際に任意のずり速度を設定できるのが特徴です。
次に、生体内の環境を模して流速のある条件で血小板接着や血栓形成の様子を観察します。これは抗凝固剤と蛍光色素で処理したキメラマウス血液を、コラーゲンを固相化したガラスキャピラリーチューブ内に流し、血栓が形成される様子を見る実験系です。血液を流す際に任意のずり速度を設定できるのが特徴です。
我々のフローシステムは手持ちの蛍光顕微鏡に三活と延長チューブ、シリンジ、シリンジポンプ等を組みあわせて作った、見るからに安普請なものです。従って形成された血栓の量を蛍光輝度で評価するような高等な装置は無く、血栓をどのように定量化するかが問題でした。血栓をライシスバッファで溶かし、actinの量やPLCgamma2の量をwesternblotで比べたりしましたが、上手く行きません。
そんなとき、我が山梨大学医学部にも共用のOlympus社のレーザー顕微鏡があることを思い出しました。FV1000 system。これでキャピラリーチューブ内の血栓を連続断層撮影すれば、Z軸方向の情報を得る事が出来そうです。装置さえあれば後は何とかなるものです。フローシステムを使った実験後直ちにキャピラリーを加工、固定し、部屋を移動して今度はレーザー顕微鏡で連続断層撮影をするという戦法で実験を行いました。
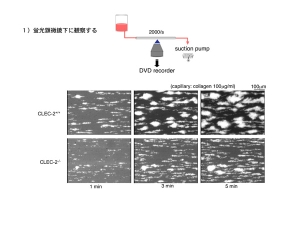 先ずは蛍光顕微鏡でのフローの実験です。実験は血管壁傷害部位に相当する2000/sのずり速度を負荷して行いました。これだとマウス1匹の血液で約5分の観察が可能です。
先ずは蛍光顕微鏡でのフローの実験です。実験は血管壁傷害部位に相当する2000/sのずり速度を負荷して行いました。これだとマウス1匹の血液で約5分の観察が可能です。
実験の結果はfigureの如く健常キメラマウスに比べ、CLEC-2欠損キメラマウスの血液ではコラーゲン上での血栓形成が若干乏しく、fragileな印象でした。楽しい結果です。
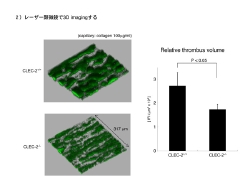 次は大至急レーザー顕微鏡での観察です。FV1000の使用は予約制ですが、使用開始予定の時刻を過ぎても使われていないと予約なしで実験に入られてしまう事もある人気の機材です。殺気だって早歩きで移動します。撮影条件を決め、撮影開始。
次は大至急レーザー顕微鏡での観察です。FV1000の使用は予約制ですが、使用開始予定の時刻を過ぎても使われていないと予約なしで実験に入られてしまう事もある人気の機材です。殺気だって早歩きで移動します。撮影条件を決め、撮影開始。
得られたデータは3D再構築し、画像当たりの積算蛍光輝度を計測します。当初蛍光輝度の積算をどうしようと考え、市販のソフトや解析サービスを探しましたが、予算オーバーなくらいのコストがかかる事がわかりました。しかしFV1000は附属のソフトでもこの程度の解析は可能です。素晴らしいです。
このようにして血栓の量を疑似定量化してみると、CLEC-2欠損キメラマウスの血栓の量は健常キメラマウスの場合の2/3程度であることがわかりました。画像で見た場合はもう少し差が大きいように思えますが、レーザーの出力や検出器の感度を調整すれば、もう少し差が明らかになるかもしれません。ともかくコラーゲン上での血栓形成は、CLEC-2が無いと抑制される事がわかりました。
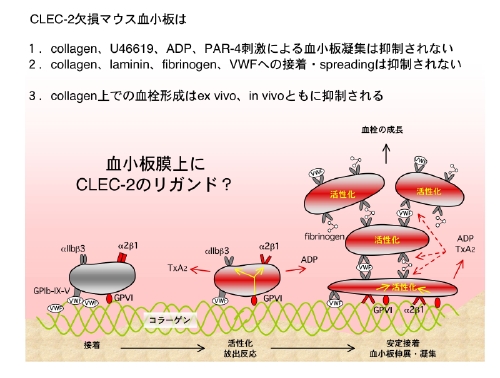 CLEC-2はコラーゲン受容体ではありませんし、コラーゲンへのadhesionやspreadingはCLEC-2欠損血小板でも健常血小板でも差がありません。しかし血栓の形成はCLEC-2欠損キメラマウス血液で抑制されます。これはどう解釈したらよいのでしょうか。やはり血栓を形成する物質に対してCLEC-2が結合し、血栓を安定化している、と考えるのが自然です。血栓の主役、血小板膜上にCLEC-2の新たなリガンドがあるのではないか。
CLEC-2はコラーゲン受容体ではありませんし、コラーゲンへのadhesionやspreadingはCLEC-2欠損血小板でも健常血小板でも差がありません。しかし血栓の形成はCLEC-2欠損キメラマウス血液で抑制されます。これはどう解釈したらよいのでしょうか。やはり血栓を形成する物質に対してCLEC-2が結合し、血栓を安定化している、と考えるのが自然です。血栓の主役、血小板膜上にCLEC-2の新たなリガンドがあるのではないか。
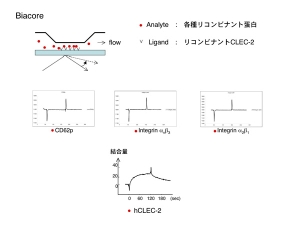 今度は血小板に新たなCLEC-2のリガンド がある可能性が浮上しました。またまた楽しくなってきました。結合するか見ればよいので、今回はBIACOREを用いてCLEC-2と血小板膜上蛋白の結合を観察する事にします。BIACOREは私たちの研究室が愛用する共用の機材で、表面プラズモン共鳴という現象を利用した装置です。センサーチップ上の金膜にリガンドを固相化し、アナライト(固相化したリガンドに結合するか調べたい物質)を流路に流します。リガンドとアナライトが結合すると、金膜に当たっていた光の共鳴角が変化し、その変化量で結合量や解離スピードを数値化する装置です。実際は難しい事は全てシステム任せなので、実験者は装置の前にいて、リガンドの固相化、アナライトの添加、数値化されたデータの解析等をマニュアル通りに行うだけです。我々の研究には非常にありがたい装置です。
今度は血小板に新たなCLEC-2のリガンド がある可能性が浮上しました。またまた楽しくなってきました。結合するか見ればよいので、今回はBIACOREを用いてCLEC-2と血小板膜上蛋白の結合を観察する事にします。BIACOREは私たちの研究室が愛用する共用の機材で、表面プラズモン共鳴という現象を利用した装置です。センサーチップ上の金膜にリガンドを固相化し、アナライト(固相化したリガンドに結合するか調べたい物質)を流路に流します。リガンドとアナライトが結合すると、金膜に当たっていた光の共鳴角が変化し、その変化量で結合量や解離スピードを数値化する装置です。実際は難しい事は全てシステム任せなので、実験者は装置の前にいて、リガンドの固相化、アナライトの添加、数値化されたデータの解析等をマニュアル通りに行うだけです。我々の研究には非常にありがたい装置です。
入手できた血小板関連のリコンビナント蛋白を順番に固相化したリコンビナントCLEC-2の上に流しますが、結合曲線は平坦なままで結合無し。figureの3つ以外にも試したのですが、何れもスカでした。
なんと最後に捨て鉢になって添加したリコンビナントCLEC-2だけが結合を示したのでした。
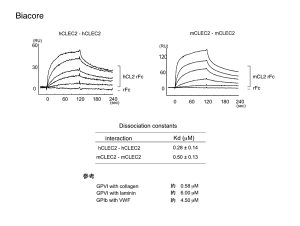 CLEC-2のホモフィリックな結合は驚きでした。しかし添加するCLEC-2の濃度を振っていくと濃度依存的に結合が増します。コントロール部位への非特異的な結合を差し引いた結果なので、特異的な結合と考えて良さそうです。CLEC-2はなんと血小板膜上のCLEC-2とホモフィリックに結合するのです。
CLEC-2のホモフィリックな結合は驚きでした。しかし添加するCLEC-2の濃度を振っていくと濃度依存的に結合が増します。コントロール部位への非特異的な結合を差し引いた結果なので、特異的な結合と考えて良さそうです。CLEC-2はなんと血小板膜上のCLEC-2とホモフィリックに結合するのです。
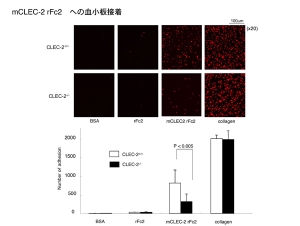 CLEC-2同士のホモフィリックな結合は、血小板レベルでも機能するのでしょうか。 答えはYESでした。CLEC-2を固相化し、その上に健常キメラマウス血小板を滴下すると、血小板接着が保持されます。しかし、CLEC-2欠損キメラマウス血小板を滴下した場合は、CLEC-2への血小板接着は明らかに抑制されます。このことから、BIACOREで観測されたCLEC-2同士のホモフィリックな結合は、血小板レベルでも機能している可能性が示唆されます。
CLEC-2同士のホモフィリックな結合は、血小板レベルでも機能するのでしょうか。 答えはYESでした。CLEC-2を固相化し、その上に健常キメラマウス血小板を滴下すると、血小板接着が保持されます。しかし、CLEC-2欠損キメラマウス血小板を滴下した場合は、CLEC-2への血小板接着は明らかに抑制されます。このことから、BIACOREで観測されたCLEC-2同士のホモフィリックな結合は、血小板レベルでも機能している可能性が示唆されます。
但しCLEC-2欠損血小板でもCCLEC-2上に接着が認められる事から、血小板膜上にはさらに異なるリガンドが存在する可能性があります。まだまだ知りたい事が尽きません。
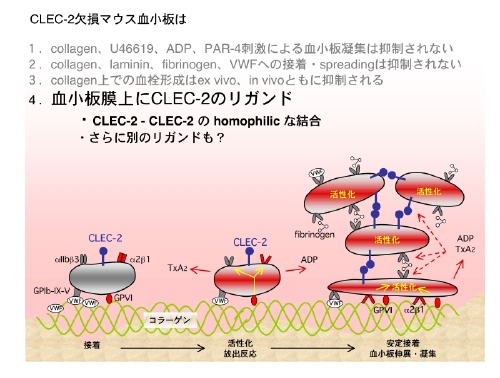 今回の結果をまとめると、figureのイラストの様になります。CLEC-2は血栓の成長や安定化に関わっているものと思われます。そのメカニズムとしては、CLEC-2が近接した血小板膜上のCLEC-2とホモフィリックに結合し、血栓の安定化に寄与しているからではないかと考えます。このホモフィリックな結合で、血小板はCLEC-2を介した活性化シグナルが惹起されているかもしれません。
今回の結果をまとめると、figureのイラストの様になります。CLEC-2は血栓の成長や安定化に関わっているものと思われます。そのメカニズムとしては、CLEC-2が近接した血小板膜上のCLEC-2とホモフィリックに結合し、血栓の安定化に寄与しているからではないかと考えます。このホモフィリックな結合で、血小板はCLEC-2を介した活性化シグナルが惹起されているかもしれません。
ではなぜ血流中の血小板同士はCLEC-2同士でホモフィリックに結合し凝集塊を作らないのでしょうか。これは、CLEC-2同士の結合が血小板活性化依存的に生じるためと思われます。具体的のどの様な変化が生じるのかは不明ですが、マウス血小板を刺激し活性化させるとCLEC-2固相化面への血小板接着が有意に増加するが、非活性化状態ではコントロールへの非特異的接着と有意差のでない程度の接着しか見られません。この辺りのデータは是非とも下記リンク先の論文(Suzuki-Inoue et.al., JBC 2010)をご覧下さい。
BIACOREでは特に活性化した状態のCLEC-2を使用したわけではありませんが、固相化すると結合活性がでるvon Willebrand Factorと同様固相化した事で物理的に構造変化が生じたのではないかと思われます。
血小板CLEC-2は血栓の安定化に関わっている事がわかりました。
今回ご紹介しませんでしたが、2009年にBloodに報告されたMayらの論文”CLEC-2 is an essential platelet-activating receptor in hemostasis and thrombosis.”(May et.al., Blood 15;114(16):3464-72)も同様の所見が記されています。彼らはCLEC-2発現を減らす抗CLEC-2抗体を健常マウスに注射し、疑似CLEC-2欠損マウス(CLEC-2 depletion マウス)を作り、これを用いて検討しています。異なる実験系で同様の結果が出ているので、CLEC-2の血栓形成・安定化で一定の役割を演じている事にはほぼ間違いないと思います。
かの論文との相違点は、MayらはCLEC-2 depletion マウスは出血が止まるまでの時間が非常に延長すると言っています。つまりCLEC-2を機能しなくすると出血した際に血が止まらないと。しかし我々のマウスではCLEC-2欠損キメラマウスでは出血時間の延長が殆ど延長しません。正確に言うと、出血時間が延長する傾向はありましたが、有意差が出ないレベルでした。Mayらのモデルでは、抗CLEC-2抗体が血小板以外のCLEC-2にも作用する事が考えられます。例えば好中球ですが、好中球のCLEC-2に抗CLEC-2抗体が結合すれば、CLEC-2を介したシグナルが発生し、TNFalpha等のサイトカイン産生が惹起される可能性があります。TNFalphaは血栓形成抑制作用があるとの報告もあり、Mayらの実験系でCLEC-2 depletion マウスの出血時間延長を引き起こす原因になったのかもしれません。
その点、私たちのマウスモデルは純粋にCLEC-2の欠損モデルです。CLEC-2を欠損させても、血栓形成は抑制しますが、出血傾向は来しません。これは抗血小板薬としては非常に優れた、理想的な特質だと思うのです。され、本研究がCLEC-2を標的とした創薬に繋がりますでしょうか。
CLEC-2の機能的役割の一部が解明でき、大学院時代からの胸のつかえが取れた気持ちです。しかしまだまだ疑問が山積。CLEC-2とは今後も長いつき合いになりそうです。
論文はこちら
Suzuki-Inoue et.al., JBC, 2010
ご協力頂いております諸先生方です。いつもありがとうございます。

その他のCLEC-2関連情報
知れば知るほど面白い血小板CLEC-2の役割。続きはこちら。

 ホーム
ホーム 移動する
移動する 前のページへ
前のページへ