掲載日:2018.2.06 お知らせ
プレスリリース・難治性神経変性疾患「アレキサンダー病」の原因分子を発見

報道機関各位
山梨大学医学部
京都府立医科大学
慶應義塾大学医学部
自然科学研究機構 生理学研究所
理化学研究所
難治性神経変性疾患「アレキサンダー病」の原因分子を発見
山梨大学医学部薬理学講座 小泉修一教授、繁冨英治学部内講師、京都府立医科大学大学院医学研究科神経内科学 齋藤光象助教、吉田誠克准教授、水野敏樹教授らの研究グループは、慶應義塾大学医学部精神・神経科学教室 田中謙二准教授、生理学研究所 池中一裕教授、理化学研究所 御子柴克彦チームリーダーらと共同で、マウスを使った実験によって、アレキサンダー病(AxD)の病気の進行が、アストロサイト[1]と呼ばれる脳細胞のCa2+シグナル興奮性[2]が高くなることにより引き起こされることを明らかとしました。AxDは非常に稀な難治性神経変性疾患で、治療法が確立されていない難病です。これまでAxDは、アストロサイト特異的な分子であるGFAP[3]と呼ばれるタンパク質の遺伝子に変異があると発症することが知られていましたが、これがどのようにして病気を進行させるのかは全く不明のままでした。今回研究チームは、AxDモデルマウスを使った研究から、AxDマウスのアストロサイトが、非常に大きく頻度の高いCa2+興奮性を示すことを見出し、これをAxCaと名付けました。このAxCaが起こらないようにした遺伝子改変マウスでは、GFAPの遺伝子に異常があっても、AxCaが起こらず、さらに興味深い事に、AxDの発症が強く抑えられることが明らかとなりました。ヒトでの研究成果が待たれますが、例えGFAPの遺伝子異常があったとしても、AxCaを抑制することで、AxDの進行を抑えられる可能性が示唆されました。
本研究成果は、米国科学誌「GLIA」への掲載に先行し、平成30年2月1日午前1時(日本時間)にオンライン版として掲載されました。
つきましては、新聞紙面またテレビ等々でご紹介いただければ幸いです。なお、取材を希望される方は、事前に担当までご連絡をお願いいたします。
背景
アレキサンダー病は、非常に稀な神経変性疾患であり、日本における患者数は約50名と推測されています。従って、原因解明や治療法開発が進んでいませんが、ほぼすべての患者さんでアストロサイトに特異的に発現するグリア線維性酸性タンパク(GFAP)をコードするGFAP遺伝子に変異が認められます。この病気は新生児から高齢者まで幅広い年齢で発症しますが、新生児や乳児期に発症する患者さんはけいれん、頭囲拡大、精神運動発達の遅れが出現し、10歳に満たず亡くなってしまうことが多く、生命予後は不良です。成人期に発症する患者さんは新生児や乳児期に発症する患者さんと比べると生命予後は良好ですが、四肢の運動障害や嚥下障害、排尿困難など日常生活に大きな支障をきたし機能予後は不良なことが多いです。
これまで遺伝子改変モデルマウスや株化細胞モデルを用いたアレキサンダー病の病態解明研究によりGFAP遺伝子変異がGFAP凝集過程を惹起し、アストロサイトの細胞機能異常を引き起こすことが報告されてきました。しかし、GFAPの遺伝子異常からどの様にしてこの病気が発症し、また進行していくのかについては不明のままで、また有効な治療法も見つかっておりません。
アストロサイトは、神経細胞および他のグリア細胞と連携することにより、中枢神経系の栄養代謝、血流調節、シナプス可塑性、細胞間の情報伝達機能など多彩な役割を果たしていることが明らかになっています。私たちの研究グループではこれらの役割のうち、アストロサイトCa2+シグナル興奮性を介した情報伝達機能に注目し、アレキサンダー病モデルマウスを用いて病態解明研究を行いました。これまで脳卒中、てんかん、アルツハイマー病などの神経疾患のモデル動物では、神経細胞のCa2+シグナルに変容をきたしているとの報告がされていました。しかし、グリア細胞であるアストロサイトのCa2+シグナルと疾患との関連性についての研究は殆ど解っていませんでした。今回、アレキサンダー病のモデル動物では異常な特徴のあるCa2+シグナル「AxCaシグナル」が観察され、さらにこれが病態の発症及び進行に大きく関わっていることを明らかにしました。今回のアレキサンダー病特有のCa2+シグナル異常は、さらなる病態解明と治療開発における重要な標的になるものと期待されます。
研究成果
1. アレキサンダー病モデルマウスから抽出したアストロサイトの網羅的解析
アレキサンダー病の疾患モデルマウスとして、乳児期に発症する患者さんで比較的多いR239H変異を有するヒトGFAP遺伝子のトランスジェニックマウスを用いました。このモデルマウスではアレキサンダー病の指標の1つであるGFAP発現レベルが野生型よりも顕著に上昇していました。この上昇の程度はGFAP遺伝子変異をヘミ接合でもつマウスよりホモ接合でもつマウスにおいて、幼弱時よりもアダルト時において、有意に高いことが明らかとなり、遺伝子型と時間に依存した現象であることがわかりました。またモデル動物の海馬組織から抽出精製したアストロサイトの網羅的な遺伝子発現解析を行ったところ、LCN2やC3と呼ばれる反応性アストロサイトを特徴づけるマーカーが上昇していました。
2. アレキサンダー病マウスモデルのアストロサイトは巨大で高頻度に出現する異常Ca2+シグナル「AxCaシグナル」を発生させ、これが病態の悪化を引き起こしている
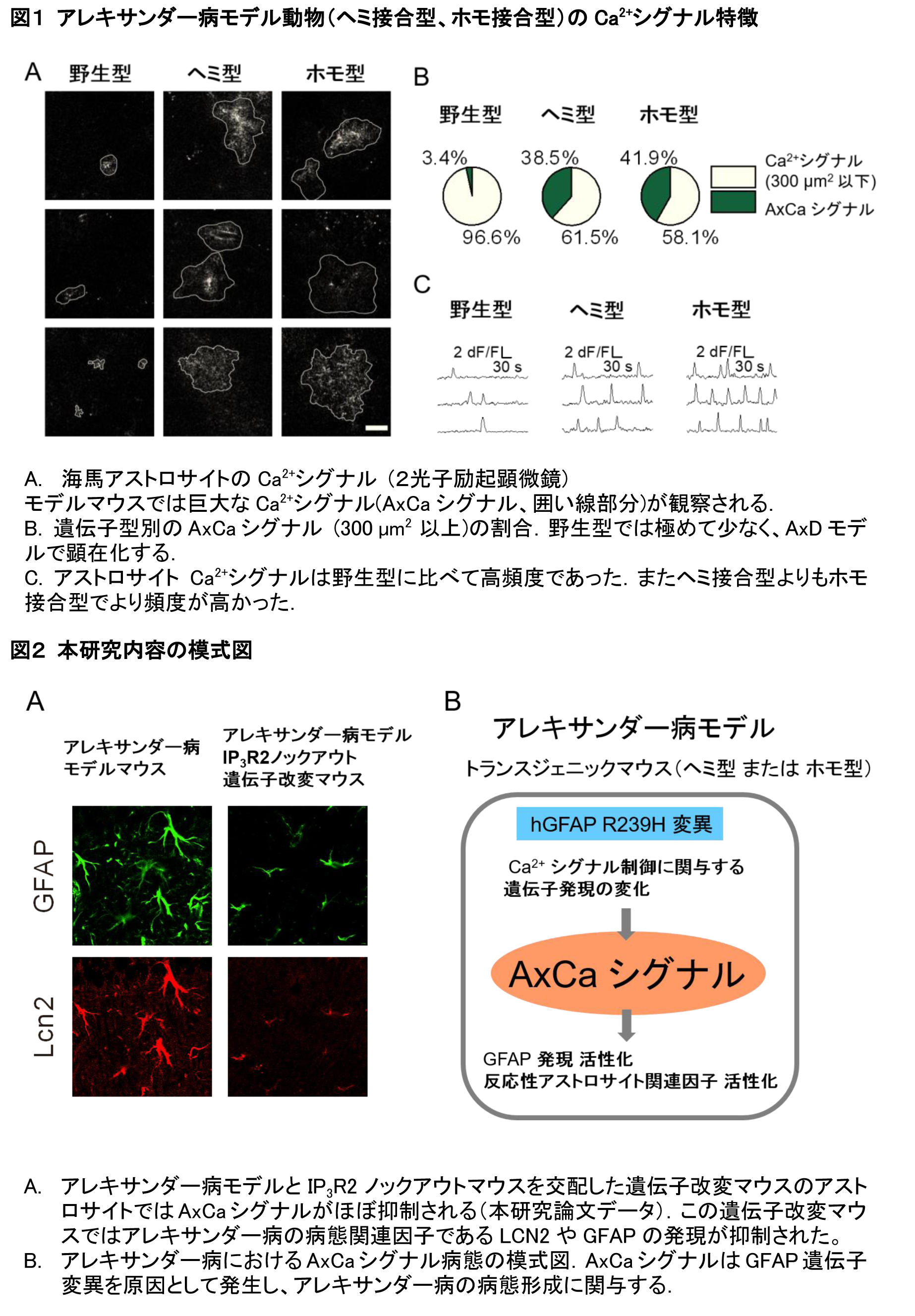
急性脳スライス実験を用いて海馬アストロサイトにて、巨大で高頻度の異常Ca2+シグナルの発生が観察されました。特に300 µm2以上の面積に拡がる大きなCa2+シグナルは特徴的であり、これを「AxCaシグナル」(aberrant extra-large Ca2+ signals)と名付けました(図1)。さらにこのAxCaシグナル活動レベルは遺伝子型、週齢に依存して増大し、またGFAP発現レベルと相関することが分かりました。
3. AxCaシグナルの抑制によりアレキサンダー病の病態関連マーカーおよびGFAPの発現レベルが抑制された
種々の薬理学的実験を行った結果、AxCaシグナルは細胞内Ca2+貯蔵に依存することが明らかとなりました。細胞内貯蔵からのCa2+放出を担う機能を持つタンパクであるイノシトール三リン酸受容体2型(IP3R2)をコードする遺伝子をノックアウトした動物モデル(IP3R2KOマウス)ではアストロサイトCa2+シグナルが大きく減少することが知られていますが、このIP3R2KOマウスと今回のアレキサンダー病モデルマウスを交配させた遺伝子改変マウスではアストロサイトからのAxCa発生が抑制されていました。さらには網羅的遺伝子発現解析から見出したLCN2やC3など病態関連マーカーおよびGFAPの発現レベルが抑制されていることが分かりました(図2)。以上の結果よりAxCaシグナルはアレキサンダー病の病態における重要因子であり、有望な治療開発標的となりうると期待されます。
本研究は、日本学術振興会 新学術領域研究「グリアアセンブリの動作原理の解明」(研究代表者:小泉修一教授)、挑戦的萌芽研究、基盤研究(B)、若手研究(B)、 特別研究奨励費、山梨大学最先端脳科学研究による支援を受けて行われました。
今後の展開
本研究によって、アレキサンダー病の病態にアストロサイトの異常なCa2+シグナル活動「AxCaシグナル」が関与することを明らかにしました。また、この異常なCa2+シグナル活動を抑制することによりGFAP遺伝子異常が存在しても病態が抑制される可能性が示唆されました。今後は、AxCaシグナルが発生する機序、AxCaシグナルがGFAPや他の病態関連因子の発現を誘導する詳細なメカニズムを解明し、そのコントロールを可能とする薬物を探索することによりヒトのアレキサンダー病に対する治療戦略を開発したいと考えています。
用語説明
[1] アストロサイト
グリア細胞は、脳内に存在する神経細胞以外の細胞群であり、アストロサイトはグリア細胞の一種。神経細胞周囲に豊富に存在し、神経細胞の物理的支持、栄養代謝供給などを担う。近年、アストロサイトも伝達物質を放出し、神経伝達機能に影響を及ぼすことが判明した。一方、脳外傷、脳卒中、てんかん、中枢神経感染症、神経変性疾患などの様々な病態時において活性化状態へ移行し、その形態・性質を変化させる。
[2] Ca2+シグナル興奮性
アストロサイトは、神経細胞のように電気的な興奮性を示さない一方で、Ca2+細胞内イオン濃度変化を利用してCa2+シグナル応答を形成すると考えられる。それによりアストロサイトは情報伝達を行い、ニューロン活動や脳機能全体と相互に作用し合っていると推定される。
[3] GFAP
アストロサイトに選択的に発現する蛋白質の一つであり、代表的なアストロサイトマーカーの一つ。中間径フィラメントと呼ばれる細胞骨格を形成する線維の構成成分。何らか病態ストレスによりアストロサイトにおいてGFAP発現が活性化し、反応性アストロサイト、さらにはアストログリオーシスと呼ばれる状態に遷移する。
論文情報
〈論文タイトル・著者情報〉
Aberrant astrocyte Ca2+ signals “AxCa signals” exacerbate pathological alterations in an Alexander disease model
Kozo Saito#, Eiji Shigetomi#, Rei Yasuda, Ryuichi Sato, Masakazu Nakano, Kei Tashiro, Kenji F. Tanaka, Kazuhiro Ikenaka, Katsuhiko Mikoshiba, Ikuko Mizuta, Tomokatsu Yoshida#, Masanori Nakagawa, Toshiki Mizuno and *Schuichi Koizumi *責任著者、#共同第1著者
米国科学誌「GLIA」に掲載されるのに先行し、 オンライン版(2018年2月1日(木) 日本時間午前1時)に掲載されました
掲載URL: http://onlinelibrary.wiley.com/journal/10.1002/(ISSN)1098-1136
|
<研究に関する問合せ> 国立大学法人 山梨大学 医学部 薬理学講座 教授 小泉 修一(コイズミ シュウイチ) Tel: 055-273-9503 Fax: 055-273-6739 携帯: 090-7849-8987 E-mail: skoizumi[at]yamanashi.ac.jp
京都府立医科大学大学院医学研究科 神経内科学 助教 齋藤光象(サイトウ コウゾウ) Tel:075-251-5793 Fax:075-211-8645 E-mai:saitok[at]koto.kpu-m.ac.jp
<報道に関する問合せ> 国立大学法人 山梨大学 総務部総務課広報企画室 Tel: 055-220-8006 Fax: 055-220-8799 E-mail:koho[at]yamanashi.ac.jp
京都府立医科大学研究支援課 Tel: 075-251-5275 Fax: 075-251-5275 E-mail: kouhou[at]koto.kpu-m.ac.jp
慶應義塾大学信濃町キャンパス総務課 広報担当 Tel: 03-5363-3611 E-mail: med-koho[at]adst.keio.ac.jp
大学共同利用機関法人 自然科学研究機構 生理学研究所 研究力強化戦略室 Tel: 0564-55-7722 Fax: 0564-55-7721 E-mail: pub-adm[at]nips.ac.jp
理化学研究所 広報室 報道担当 Tel: 048-467-9272 Fax: 048-462-4715 E-mail: ex-press[at]riken.jp [at]部分は@に置き換えて下さい. |

